Содержание статьи:
- 1 Инструкция по применению циклоферона в таблетках, раствора для инъекций
- 2 Состав, физико-химические свойства, цена
- 3 Фармакологическое действие
- 4 Противопоказания
- 5 Особые указания
- 6 Инструкция по применению циклоферона
- 7 Побочные эффекты
- 8 Лекарственное взаимодействие
- 9 Тромбоцитопения – причины и симптомы заболевания. Тромбоцитопения при беременности
- 10 Что такое тромбоцитопения?
- 11 Причины и патогенез тромбоцитопении
- 12 Степени тромбоцитопении
- 13 Тромбоцитопения при беременности
Инструкция по применению циклоферона в таблетках, раствора для инъекций
Циклоферон – популярное противовирусное лекарственное средство отечественного производства, повышающее резистентность организма. Является высокомолекулярным активатором образования интерферона и отличается широчайшим спектром фармакологической активности.
Высокая терапевтическая активность лекарственного средства обусловлена спектром биологического действия. Эффективен в терапии заболеваний вирусной природы, в том числе, гриппа, также практикуется назначение циклоферона при некоторых бактериальных инфекциях, как иммуностимулятора. Традиционно применяется при иммунодефицитах различной степени выраженности, включая ВИЧ-инфекцию. Характеризуется противоканцерогенным эффектом и подавляет развитие аутоиммунных реакций, что еще больше расширяет терапевтический спектр препарата.
Циклоферон присутствует на фармрынке более 20 лет, отличается доступной ценой в своем сегменте и является препаратом выбора при иммунодефицитах, а также при болезнях вирусной природы.
Состав, физико-химические свойства, цена
Препарат производится в 3х лекарственных формах: линимент для местного наружного применения, таблетки пероральные и парентеральный раствор.
Фармакологическое действие
Циклоферон оказывает 2 выраженных эффекта: противовирусный и иммуномодулирующий, а также противовоспалительное, антипролиферативное (подавляюще избыточный рост клеток) и противоопухолевое действие. В организме меглумин акридонацетат потенцирует синтезирование и аккумуляцию в органах и тканях значительных титров интерферонов α и β. При этом наибольшее содержание интерферонов отмечается в структурах, богатых лимфоидной тканью: селезенка, легкие, слизистая кишечника, печень.
Циклоферон активирует костномозговые стволовые клетки, обеспечивает образование гранулоцитов. Нормализует соотношение Т-супрессоров, подавляющих образование антигенов, и Т-хелперов, усиливающих адаптивный иммунный ответ. Активирует клетки-киллеры и Т-лимфоциты. Такой эффект особенно важен при иммунодефицитах различной природы, поскольку приводит к коррекции иммунного статуса. Проникает в ткани головного мозга.
Таким образом, циклоферон:
- приводит к выраженному улучшению при распространенных вирусных болезнях как грипп, герпес, энтеровирусная инфекция, и при менее распространенных патологиях: клещевом энцефалите, гепатитах, цитомегаловирусной и папилломатозной инфекциях;
- нормализует иммунный статус у ВИЧ-инфицированных;
- оказывает антимикробное и антихламидийное действие;
- предупреждает запуск опухолевых процессов благодаря антиметастатическому и противоканцерогенному эффектам;
- подавляет аутоиммунные реакции, уменьшая тем самым выраженность боли и воспалительных явлений при ревматических болезнях и системных патологиях соединительной ткани;
- вызывает улучшение баланса иммунитета, при местном применении характеризуется антипролиферативным действием и быстрым устранением воспаления.
Фармакокинетика
После орального приема через 2-3 ч достигает максимальной плазменной концентрации. Постепенно концентрация препарата снижается и через сутки циклоферон обнаруживается в организме в остаточном количестве.
Период полувыведения – 4-5 ч. В терапевтических дозировках кумуляции меглумина акридонацетата не наблюдается.
Таблетки назначаются в комплексной терапии у взрослых при:
- гриппе и ОРЗ;
- герпесах;
- ОКИ вирусной этиологии;
- нейроинфекциях, включая клещевой боррелиоз и энцефалит, серозный менингит;
- вторичном иммунодефиците на фоне хронических инфекций, вызванных грибками и бактериями;
- гепатитах С и В (хронических);
- ВИЧ-инфекции в стадии 2А-3В;
У детей таблетки циклоферона применяются в составе комплексной терапии при:
- инфекции герпетической этиологии;
- гепатитах С и В (и острых, и хронических);
- ВИЧ-инфекции в стадии 2А-3В;
- вирусных кишечных инфекциях;
- ОРЗ и гриппе, а также для их предупреждения.
Раствор, как лекарственное средство комплексной терапии, показан для лечения взрослых пациентов при следующих состояниях:
- ВИЧ-инфекции в стадии 2А-3В;
- гепатитах С, D, А, В;
- системных болезнях соединительной ткани и заболеваниях ревматического характера (ревматоидный артрит, СКВ);
- нейроинфекциях, в т.ч. при клещевом боррелиозе и энцефалите, серозном менингите;
- инфекциях, вызванных цитомегаловирусом и вирусом герпеса;
- вторичном иммунодефиците вследствие грибковых и бактериальных инфекций, острых и хронических;
- хламидийных инфекциях;
- патологиях суставов (дегенеративно-дистрофических), в т.ч. при деформирующем остеоартрозе.
У детей от 4 лет парентеральное применение циклоферона показано при:
- гепатитах вирусных С, А, D, GP и В;
- ВИЧ-инфекции (стадия 2А-3В);
- герпетической инфекции.
Линимент циклоферон является компонентом комплексной терапии и применяется местно у взрослых при:
- герпетической инфекции;
- вагинозах неспецифических и вагититах бактериальных;
- уретритах специфических (гонорейном, кандидозном, хламидийном, трихомонадном), баланопоститах, а также при неспецифических уретритах.
Противопоказания
- Цирроз печени декомпенсированный – для таблеток и раствора;
- Гиперчувствительность к составляющим всех лекарственных форм;
- Детский возраст до 4 лет (раствор и таблетки) и до 18 лет (линимент);
Многих интересует, можно ли циклоферон при беременности и лактации. Ответ однозначен – все формы препарата противопоказаны.
Особые указания
С осторожностью применяется при эрозиях, гастритах, язвах желудка/12перстной кишки, дуоденитах в стадии обострения, а также при сильных аллергических реакциях.
Лечение раствором и таблетками при дисфункции щитовидки должно проводиться с участием и контролем эндокринолога.
Не затормаживает скорость реакции.
Инструкция по применению циклоферона
Таблетки, для взрослых
Препарат принимают однократно/сут, за полчаса до еды, не измельчая и запивая водой. Доза зависит от заболевания и возраста.
- Герпетическая инфекция. В дозе 2-4 табл. по схеме: на 1й, 2й, 4й, 6й, 8й, 11й, 14й, 17й, 20й и 23й дни – это базовая схема, подходящая для большинства патологий. На курсовое лечение – 20-40 табл. Начинают лечение при обострении заболевания;
- ОРИ и грипп. Взрослые по 2-4 табл. однократно/сут, 10-20 табл. на курс с первых симптомов. При тяжелом гриппе разовая доза увеличивается до 6 табл. Назначают и другие препараты для симптоматического лечения (жаропонижающие и др.);
- Хронические гепатиты С и В. По 4 табл. по базовой схеме, затем – по 4 табл. однократно в 3-5 дней порядка 3,5 мес. На курс необходимо 100-150 табл. При лечении гепатита С или микст-инфекции назначаются повторные курсы, в комплексе с иными противовирусными и интерфероном;
- Кишечные инфекции (как составляющее комплексного лечения): по 2 табл. на прием по базовой схеме до 8го дня, а с 11го — по 4 табл.;
- Нейроинфекции. В дозе по 4 табл. по базовой схеме, далее – по 4 табл. через 5 дней. Курс лечения 2,5 мес;
- ВИЧ-инфекция. В дозе по 4 табл. по базовой схеме, затем в такой же дозе 1 раз в 3-5 дней в течение 2,5 мес. Через 2-3 недели курс повторяют (на курс уходит 100-150 табл.);
- Иммунодефициты. По 2 табл. по базовой схеме.
Как принимать циклоферон в детском возрасте
Препарат принимают однократно в сут., за полчаса до еды, запивая водой.
- Дети 4-6 лет: на прием по 1 табл.;
- Дети 7-11 лет: на прием по 2 табл.;
- Дети с 12 лет: на прием по 3 табл.
Схема лечения зависит от патологии:
- Острые вирусные гепатиты С, В: рекомендуемая доза по возрасту двукратно через 1 день, затем переходят на трехразовый прием через 48 ч, а далее – 5 приемов ч/з 72 ч;
- Хронические вирусные гепатиты С и В: в рекомендуемых дозах по возрасту через 48 ч, на курс 50-150 табл;
- ВИЧ-инфекция: доза возрастная на 1, 2, 4, 6, 8, 11, 14, 17, 20 дни, потом по поддерживающей схеме однократно в 3-5 дней порядка 5 мес.;
- Герпетическая инфекция: 1, 2, 4, 6, 8, 11, 14 дни — в возрастной дозе, далее – исходя из тяжести патологии;
- Кишечные инфекции: однократно в сут. в возрастной дозе на 1, 2, 4, 6, 8, 11 дни (6-18 таблеток на курс);
- Грипп и ОРЗ: в возрастных дозах с суточным интервалом, 5-9 приемов циклоферона на курс лечения;
- Во время неблагоприятной ситуации по гриппу и другим ОРВИ для их профилактики: возрастная доза, которая принимается на 1, 2, 4, 6, 8 день, далее еще 5 раз через 72 часа. Профилактический курс: 10-30 таблеток.
Схема применения инъекций циклоферона у взрослых
Раствор вводят в/в или в/м однократно в сут. по базовой схеме: на 1, 2, 4, 6, 8, 11, 14, 17, 20, 23, 26, 29 день. Доза зависит от патологии.
- Вирусные гепатиты В, А, D, С. Однократная доза – 250-500 мг, на курс общая суммарная доза 2,5-5 гр. Всего назначают 10 инъекций, через 2 нед. курс повторяют;
- Инфекции, ассоциированные с герпесом и цитомегаловирусом: 10 инъекций по 250 мг (общая доза на курс 2,5 гр). Наиболее эффективно работает при лечении в самом начале обострения;
- Нейроинфекции. 12 инъекций в дозе 250-500 мг. Лечение комбинируется с этиотропной терапией. Общая доза: 3-6 г. Допускается повторное лечение;
- ВИЧ-инфекция. Разовая доза — 500 мг, вводят в/м 10 уколов по базовой схеме. Поддерживающее лечение, которое назначают после курса: по 500 мг однократно в 5 дней 2,5 месяца. Через 30 дней после окончания — повторный терапевтический курс;
- Хламидийные инфекции. По 250 мг, 10 уколов на курс. Повторное лечение проводят через 2 нед. после окончания курса. В данном случае рекомендуется применять циклоферон вместе с антибиотиками;
- Иммунодефицитные состояния. По 250 мг внутримышечно, 10 инъекций. Через 6-12 мес. рекомендован повторный курс;
- Системные патологии соединительной ткани и ревматические заболевания. По 5 инъекций в течение 4 курсов (через 10-14 дней), в разовой дозе 250 мг. Повторные курсы назначаются врачом;
- Болезни опорно-двигательной системы дегенеративно-дистрофического характера. По 250 мг – 2 курса по 5 уколов, с промежутком 10-14 дней;
Смотрите так же: Инструкция вакцины против сибирской язвы для человека
Схема применения инъекций циклоферона у детей
Доза раствора циклоферона рассчитывается индивидуально: 6-10 мг/кг массы тела ребенка. Вводят внутримышечно либо внутривенно, однократно в сут.
- Острые гепатиты В, С, А, GP, D и микст-формы: доза, исходя из массы тела, которую вводят на 1, 2, 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28 дни. При затяжной инфекции через 14 дней повторяют по той же схеме;
- Хронические гепатиты С, В, GP, D. Доза по массе тела, которую вводят на 1, 2, 4, 6, 8, 10, 12, 14, 16, 18-й день, далее назначается поддерживающая схема на 3 месяца по 1 инъекции через 3 дня;
- ВИЧ-инфекция. Вводят по схеме терапии гепатитов хронических, далее: поддерживающая схема однократно в 5 дней 3 месяца;
- Герпетическая инфекция. Рассчитанную на вес дозу вводят на 1, 2, 4, 6, 8, 11, 14, 17, 20, 23-день, после для поддержания эффекта: по 1 инъекции через 5 дней.
Схема циклоферона – местное применение
- Герпетическая инфекция. Линимент наносят на область поражения тонким слоем, однократно в сут., в течение 5 дней. При генитальном герпесе делают ежедневные внутриуретральные либо интравагинальные инстилляции 5 мл линимента (1 флакон) 1 раз в сут. 10-15 дней. Линимент допускается комбинировать с другими общими и местными противогерпетическими средствами;
- Кандидозные, неспецифические уретриты. Делают инстилляции 5-10 мл линимента (объем 1-2 флаконов) в уретру. Доза варьируется от тяжести поражения.
- при развитии воспаления в переднем отделе уретры у мужчин канюлю шприца с линиментом погружают в наружное отверстие канала, затем аккуратно сжимают отверстие на 1,5-3 минут. Инстилляционный раствор через некоторое время выделяется самотеком. Помочиться нужно через полчаса (иначе может развиться отек слизистой).
- при поражении семенных желез либо заднего отдела уретры проводят внутриуретральные инстилляции линимента с помощью уретрального катетера по 5-10 мл 10-14 дней подряд, однократно в сутки.
- при лечении специфических уретритов обязательно применение антибактериальных средств, к которым чувствительна патогенная флора.
- Кандидозный и неспецифический кольпит, вагиноз бактериальный, эндоцервицит. Назначают инстилляции линимента во влагалище по 5-10 мл ежедневно, 10-15 дней. Для того, чтобы линимент не вытекал, следует затампонировать вход во влагалище небольшим стерильным тампоном на 2-3 часа.
- При диагностировании сочетанной интрауретральной и интравагинальной инфекции следует применять инстилляции и во влагалище, и в уретру по 5 мл 10-15 дней. Допускается введение пропитанных стерильных тампонов.
Линимент сочетаем с вагинальными формами препаратов (суппозитории, таблетки), поэтому может применяться в комплексе при хронической патологии женской половой сферы.
Предложенные выше схемы лечения являются базовыми и могут варьироваться в индивидуальном порядке.
Побочные эффекты
Возможно проявление общих и местных реакций гиперчувствительности.
Лекарственное взаимодействие
Препарат на 100 % совместим с иными лекарствами, которые традиционно применяются в терапии указанных болезней, включая интерфероны, химиотерапевтические и симптоматические средства. Отмечено усиление эффектов аналогов нуклеозидов и интерферонов при совместном применении с циклофероном.
Одним из положительных эффектов циклоферона является уменьшение выраженности побочного действия интерферонотерапии и химиотерапии.
Аналогов по составу на данный момент не зарегистрировано.
Тромбоцитопения – причины и симптомы заболевания. Тромбоцитопения при беременности
Что такое тромбоцитопения?
Тромбоцитопения – патологическое состояние, характеризующееся снижением количества тромбоцитов (красных кровяных пластинок) в кровяном русле до 140 000/мкл и ниже (в норме 150 000 – 400 000/мкл).
Морфологически тромбоциты представляют собой лишенные ядра небольшие фрагменты мегакариоцитарной цитоплазмы. Это самые маленькие кровяные элементы, которые происходят от мегакариоцита – самого крупного клеточного предшественника.
Красные кровяные пластинки образуются путем отделения участков материнской клетки в красном костном мозге. Этот процесс недостаточно изучен, однако известно, что он является управляемым – при повышенной потребности в тромбоцитах резко увеличивается скорость их образования.
Продолжительность жизни тромбоцитов относительно невелика: 8-12 дней. Старые дегенеративные формы поглощаются тканевыми макрофагами (около половины красных кровяных пластинок заканчивает свой жизненный цикл в селезенке), а на их место из красного костного мозга поступают новые.
Несмотря на отсутствие ядра, тромбоциты обладают множеством интересных особенностей. К примеру, они способны к активному направленному амебоподобному движению и фагоцитозу (поглощению чужеродных элементов). Таким образом, тромбоциты участвуют в местных воспалительных реакциях.
Наружная мембрана тромбоцитов содержит специальные молекулы, способные распознавать поврежденные участки сосудов. Обнаружив мелкое повреждение в капилляре, кровяная пластинка прилипает к пораженному участку, встраиваясь в выстилку сосуда в виде живой заплатки. Поэтому при снижении количества тромбоцитов в кровяном русле возникают множественные мелкие точечные кровоизлияния, называемые диапедезными.
Однако самая главная функция тромбоцитов состоит в том, что они играют ведущую роль в остановке кровотечения:
- формируют первичную тромбоцитарную пробку;
- выделяют факторы, способствующие сужению сосуда;
- участвуют в активации сложной системы свертывающих факторов крови, что в конечном итоге приводит к формированию фибринового сгустка.
Поэтому при значительной тромбоцитопении возникают опасные для жизни кровотечения.
Причины и патогенез тромбоцитопении
Снижение образования тромбоцитов в красном костном мозге
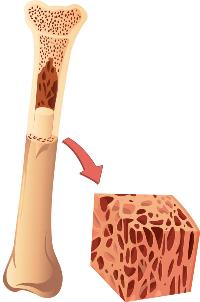 Тромбоцитопении, связанные со сниженным образованием тромбоцитов в красном костном мозге, в свою очередь можно разделить на следующие группы:
Тромбоцитопении, связанные со сниженным образованием тромбоцитов в красном костном мозге, в свою очередь можно разделить на следующие группы:
- тромбоцитопении, связанные с гипоплазией мегакариоцитарного ростка в костном мозге (недостаточное образование клеток-предшественников тромбоцитов);
- тромбоцитопении, связанные с неэффективным тромбоцитопоэзом (в таких случаях образуется нормальное, или даже повышенное количество клеток-предшественниц, однако по тем или иным причинам нарушается образование тромбоцитов из мегакариоцитов);
- тромбоцитопении, связанные с метаплазией (замещением) мегакариоцитарного ростка в красном костном мозге.
Гипоплазия мегакариоцитарного ростка красного костного мозга (недостаточная продукция клеток-предшественников тромбоцитов)
О гипоплазии мегакариоцитарного ростка говорят в тех случаях, когда костный мозг не в состоянии обеспечить ежедневное замещение 10-13% тромбоцитов (необходимость такой быстрой замены связана с небольшой продолжительностью жизни кровяных пластинок).
Наиболее частая причина гипоплазии мегакариоцитарного ростка – апластическая анемия. При этом заболевании происходит тотальная гипоплазия всех кроветворных клеток (предшественников эритроцитов, лейкоцитов и тромбоцитов).
Гипоплазию костного мозга с развитием тромбоцитопении могут вызвать многие лекарственные препараты, такие как: левомицетин, цитостатики, антитиреоидные средства, препараты золота.
Механизмы действия лекарств могут быть различны. Цитостатики оказывают прямое угнетающее влияние на костный мозг, а левомецитин может привести к тромбоцитопении лишь в случае идиосинкразии (индивидуальной повышенной чувствительности костного мозга к данному антибиотику).
Есть экспериментальные данные, доказывающие угнетение мегакариоцитарного ростка под действием алкоголя. В таких случаях тромбоцитопения не достигает крайне низких цифр (до 100 000/мкл), не сопровождается выраженными кровотечениями и исчезает через 2-3 дня после полного отказа от приема алкоголя.
Что касается инфекций, то чаще всего гипоплазию мегакариоцитарного ростка вызывают вирусы. Описаны случаи транзиторной тромбоцитопении после вакцинации живой коревой вакциной. Иногда угнетение мегакариоцитарного ростка вызывает вирус паротита (свинки), вирусы гепатитов А, В и С.
Непосредственное цитопатическое действие на мегакариоциты оказывает также вирус иммунодефицита человека. Нередко у ВИЧ-инфицированных развивается выраженная тромбоцитопения продукции.
Иногда причиной угнетения мегакариоцитарного ростка становятся генерализованные бактериальные или грибковые инфекции (сепсис). Чаще всего такого рода осложнения развиваются в детском возрасте.
Длительная гипоксия также может приводить к угнетению мегакариоцитарного ростка и слабо выраженной тромбоцитопении.
Врожденная мегакариоцитарная гипоплазия, как правило, является следствием тяжелых наследственных заболеваний, таких как анемия Фанкони (конституциональная апластическая анемия) и др.
Смотрите так же: Из чего состоят комбикорма для кур
Крайне редко встречается врожденная амегакариоцитарная тромбоцитопения, для которой характерно изолированное поражение мегакариоцитарного ростка костного мозга. Клинические проявления этого заболевания развиваются рано, но выражены умеренно.
Приобретенная изолированная амегакариоцитарная тромбоцитопеническая пурпура также является редким заболеванием, механизм развития которого до сих пор не изучен.
Неэффективный тромбоцитопоэз, как причина тромбоцитопении (нарушение образования тромбоцитов из клеток-предшественниц)
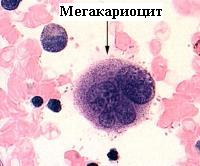 Торможение образования тромбоцитов из клеток-предшественниц также может быть вызвано несколькими причинами.
Торможение образования тромбоцитов из клеток-предшественниц также может быть вызвано несколькими причинами.
Одной из причин такого рода тромбоцитопении может быть врожденный недостаток тромбопоэтина – вещества, стимулирующего образование тромбоцитов из мегакариоцитов. Сегодня эту патологию можно распознать при помощи определения уровня тромбопоэтина в крови.
Неэффективный тромбоцитопоэз характерен для мегалобластной анемии (анемии связанной с авитаминозом В12 и/или недостатком фолиевой кислоты). В таких случаях, вследствие авитаминоза, нарушается нормальное образование кровяных пластинок. Тромбоцитопения исчезает после назначения витаминотерапии.
Тромбоцитопоэз нарушается при тяжелой железодефицитной анемии, поскольку нормальный уровень железа в крови необходим для образования тромбоцитов и усвоения витамина В12 гемопоэтическими клетками.
Кроме того, нарушение тромбоцитопоэза может быть вызвано вирусными инфекциями, хронической алкогольной интоксикацией, а также некоторыми врожденными заболеваниями, при которых тромбоцитопения сочетается с тромбоцитопатией (образованием дефектных тромбоцитов).
К таким врожденным заболеваниям относятся редкая аутосомно-доминантная аномалия Мей-Хегглина, синдромы Бернарда-Сулье и Вискота-Олдрича и др.
Метаплазия (перерождение) мегакариоцитарного ростка в красном костном мозге, как причина тромбоцитопении
Метаплазия мегакариоцитарного ростка чаще всего возникает при следующих патологических состояниях:
1. Последние стадии рака (замещение костного мозга метастазами).
2. Онкологические заболевания системы крови (замещение опухолевыми клетками):
- лейкозы;
- миеломная болезнь;
- лимфомы.
3. Миелофиброз (замещение красного костного мозга фиброзной тканью).
4.Саркоидоз (замещение специфическими гранулемами).
В таких случаях, как правило, страдают все ростки кроветворной ткани, что проявляется панцитопенией (снижением количества клеточных элементов в крови – эритроцитов, лейкоцитов и тромбоцитов).
Повышенное потребление (разрушение) тромбоцитов
Ускоренное разрушение тромбоцитов является самой частой причиной тромбоцитопении. Как правило, повышенное потребление кровяных пластинок приводит к гиперплазии костного мозга, увеличению количества мегакариоцитов и, соответственно, к повышению образования тромбоцитов. Однако когда скорость деструкции превышает компенсаторные возможности красного костного мозга, развивается тромбоцитопения.
Тромбоцитопении разрушения можно разделить на обусловленные иммунологическими и неиммунологическими механизмами.
Разрушение тромбоцитов антителами и иммунными комплексами (иммунная тромбоцитопения)
Тромбоцитопения у лиц с нормальной продукцией кровяных телец в преимущественном большинстве случаев обусловлена разрушением тромбоцитов под влиянием различных иммунных механизмов. При этом образуются антитромбоцитарные антитела, которые можно обнаружить при специальном иммунологическом обследовании.
Для всех иммунных тромбоцитопений без исключения характерны следующие признаки:
- отсутствие выраженной анемии и лейкопении;
- размеры селезенки в пределах нормы, или увеличены незначительно;
- увеличение количества мегакариоцитов в красном костном мозге;
- снижение продолжительности жизни тромбоцитов.
При этом по типу развития различают три группы иммунологических тромбоцитопений:
1. Изоиммунные — обусловленные продукцией аллоантител (антител к антигенам тромбоцитов другого организма).
2. Аутоиммунные — обусловленные продукцией аутоантител (антител к антигенам тромбоцитов собственного организма).
3. Иммунные — спровоцированные приемом лекарственных препаратов.
Иммунные тромбоцитопении, возникающее при попадании в организм «чужих» тромбоцитов
Изоиммунные тромбоцитопении возникают при попадании в организм «чужих» тромбоцитов (переливание крови, беременность). К этой группе патологий относится неонатальная (младенческая) аллоиммунная тромбоцитопеническая пурпура, посттрансфузионная пурпура и рефрактерность (устойчивость) пациентов к переливанию крови.
Неонатальная аллоиммунная тромбоцитопеническая пурпура (НАТП) возникает при антигенной несовместимости матери и ребенка по тромбоцитарным антигенам, так что в кровь плода поступают материнские антитела, уничтожающие тромбоциты плода. Это достаточно редкая патология (1:200 – 1:1000 случаев), тяжесть которой зависит от силы иммунного ответа матери.
В отличие от несовместимости матери и плода по резус фактору, НАТП может развиться во время первой беременности. Иногда тромбоцитопения у плода возникает уже на 20-й неделе внутриутробного развития.
Патология проявляется генерализованной петехиальной сыпью (точечные кровоизлияния) на коже и слизистых оболочках, меленой (дегтеобразный кал, свидетельствующий о внутренних кровотечениях), носовыми кровотечениями. У 20% детей развивается желтуха. Особую опасность представляют внутримозговые кровоизлияния, которые развиваются у каждого третьего ребенка с НАТП.
Посттрансфузионная тромбоцитопеническая пурпура развивается через 7-10 дней после переливания крови или тромбоцитарной массы, и проявляется выраженными кровотечениями, геморрагической кожной сыпью и катастрофическим падением количества тромбоцитов (до 20 000/мкл и ниже). Механизм развития этого крайне редкого осложнения до сих пор не изучен.
Рефрактерность (нечувствительность) пациентов к переливанию тромбоцитов развивается крайне редко при повторных переливаниях препаратов крови, содержащих тромбоциты. При этом уровень тромбоцитов у больных остается неизменно низким, несмотря на поступление донорских кровяных пластинок.
Аутоиммунные тромбоцитопении
Аутоиммунные тромбоцитопении связаны с преждевременной гибелью тромбоцитов в результате действия антител и иммунных комплексов, выработанных к тромбоцитам собственного организма. При этом различают первичные (идиопатические, неизвестной этиологии) и вторичные (вызванные известными причинами) аутоиммунные тромбоцитопении.
К первичным относят острую и хроническую идиопатическую аутоиммунную тромбоцитопеническую пурпуру. Ко вторичным – множество заболеваний, при которых возникают аутоантитела к кровяным пластинкам:
- злокачественные опухоли лимфоидной ткани (хронический лимфолейкоз, лимфомы, лимфогранулематоз);
- приобретенная аутоиммунная гемолитическая анемия (синдром Эванса-Фишера);
- системные аутоиммунные заболевания соединительной ткани (системная красная волчанка, ревматоидный артрит);
- органоспецифические аутоиммунные заболевания (аутоиммунный гепатит, неспецифический язвенный колит, болезнь Крона, аутоиммунный тиреоидит, анкилозирующий спондилоартрит);
- вирусные инфекции (краснуха, ВИЧ, опоясывающий герпес).
Отдельно, как правило, выделяют аутоиммунные тромбоцитопении, ассоциированные с приемом медицинских препаратов. Список лекарственных средств, способных вызвать такого рода патологическую иммунную реакцию, достаточно длинный:
- Ампициллин;
- Аспирин;
- Пенициллин;
- Бисептол;
- Рифампицин;
- Гентамицин;
- Гепарин;
- Героин;
- Морфин;
- Ранитидин;
- Циметидин;
- Фуросемид;
- Цефалексин и др.
Для такой патологии характерна выраженная геморрагическая сыпь. Заболевание самоизлечивается при отмене препарата.
Неиммунные причины разрушения тромбоцитов
Прежде всего, повышенное разрушение тромбоцитов может происходить при патологиях, связанных с нарушением состояния внутренней выстилки сосудов, таких как:
- пороки сердца;
- постоперационные изменения (искусственные клапаны, синтетические шунты сосудов и т.п.);
- выраженный атеросклероз;
- поражение сосудов метастазами.
Кроме того, тромбоцитопения потребления развивается при синдроме внутрисосудистого свертывания, при ожоговой болезни, при длительном пребывании в условиях повышенного атмосферного давления или гипотермии.
Снижение количества тромбоцитов также может наблюдаться при сильной кровопотере и массивных трансфузиях (при внутривенном вливании большого количества растворов – так называемая тромбоцитопения разведения).
Нарушение распределения тромбоцитов
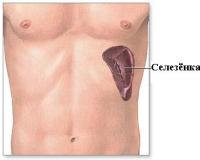 В норме от 30 до 45% активных тромбоцитов кровяного русла находятся в селезенке, которая является своеобразным депо кровяных пластинок. При повышении потребности в тромбоцитах кровяные пластинки выходят из депо в кровь.
В норме от 30 до 45% активных тромбоцитов кровяного русла находятся в селезенке, которая является своеобразным депо кровяных пластинок. При повышении потребности в тромбоцитах кровяные пластинки выходят из депо в кровь.
При заболеваниях, сопровождающихся значительным увеличением селезенки, количество тромбоцитов, находящихся в депо, значительно увеличивается, и в отдельных случаях может достигать 80-90%.
При длительной задержке тромбоцитов в депо происходит их преждевременное разрушение. Так что со временем тромбоцитопения распределения переходит в тромбоцитопению разрушения.
Чаще всего такого рода тромбоцитопения происходит при следующих заболеваниях:
- цирроз печени с развитием портальной гипертензии;
- онкологические заболевания системы крови (лейкозы, лимфомы);
- инфекционные заболевания (инфекционный эндокардит, малярия, туберкулез и др.).
Как правило, при значительном увеличении селезенки развивается панцитопения (снижение количества всех клеточных элементов крови), а тромбоциты становятся более мелкими, что помогает в диагностике.
Так, тромбоцитопения при алкоголизме обусловлена непосредственным угнетающим влиянием алкоголя на костный мозг с развитием гипоплазии мегакариоцитарного ростка, а также нарушением образования тромбоцитов из клеток-предшественниц. А в случае развития алкогольного цирроза печени с портальной гипертензией возникает спленомегалия (значительное увеличение селезенки), приводящая к тромбоцитопении перераспределения.
В случае злокачественных опухолей причиной тромбоцитопении может быть:
- вытеснение мегакариоцитарного ростка опухолевыми клетками;
- угнетение костного мозга токсинами;
- образование аутоантител к тромбоцитам с развитием иммунной тромбоцитопении разрушения;
- увеличение селезенки с возникновением тромбоцитопении перераспределения.
Тромбоцитопения является одним из ранних признаков ВИЧ-инфекции. При этом снижение количества тромбоцитов вызывается как непосредственным угнетающим влиянием вирусов на клетки мегакариоцитарного ростка, так и аутоиммунными реакциями. А при тяжелых инфекционных осложнениях — на стадии развернутого СПИД и увеличения селезенки с развитием тромбоцитопении перераспределения.
Недостатки патогенетической классификации учтены при разработке более простых вариантов.
Таким образом, все тромбоцитопении разделяются на первичные и вторичные (симптоматические). К первичным относят самостоятельные патологии (идиопатическая тромбоцитопеническая пурпура), а ко вторичным – те случаи, когда тромбоцитопения является осложнением основного заболевания (тромбоцитопения при лейкозе, циррозе печени, ВИЧ-инфекции и т.п.).
Смотрите так же: Вопросы и ответы по вич инфекциям
Кроме того, различают врожденные (неонатальная аллоиммунная тромбоцитопеническая пурпура) и приобретенные (острая или хроническая идиопатическая тромбоцитопеническая пурпура) тромбоцитопении.
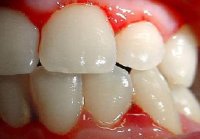 Независимо от причины возникновения тромбоцитопении, снижение количества кровяных пластинок в крови проявляется следующими симптомами:
Независимо от причины возникновения тромбоцитопении, снижение количества кровяных пластинок в крови проявляется следующими симптомами:
- склонность к внутрикожным кровоизлияниям (пурпура);
- кровоточивость десен;
- обильные менструации у женщин;
- носовые кровотечения;
- желудочно-кишечные кровотечения;
- кровоизлияния во внутренние органы.
Следует отметить, что перечисленные симптомы неспецифичны, и могут проявляться также при других патологиях. Например, при тромбоцитопатиях (продукции дегенеративных тромбоцитов), при заболеваниях сосудов микроциркуляторного русла, в том числе связанных с авитаминозом С (цинга).
Поэтому о тромбоцитопении можно говорить лишь в тех случаях, когда геморрагический синдром сопровождается снижением количества тромбоцитов в крови.
Степени тромбоцитопении
Выраженность симптомов тромбоцитопении зависит от степени снижения уровня тромбоцитов в крови. Так, если их концентрация в крови превышает 30 000 – 50 000/мкл, то заболевание может протекать субклинически.
В таких случаях возможно появление склонности к носовым кровотечениям, длительным и обильным месячным у женщин, а также к образованию внутрикожных кровоизлияний при незначительных повреждениях.
Так что легкую степень заболевания нередко обнаруживают случайно, при проведении планового обследования или исследования картины крови по поводу каких-либо других заболеваний.
При тромбоцитопении средней тяжести (20 000 – 50 000/мкл) появляется характерная геморрагическая сыпь – пурпура, которая представляет собой множественные мелкие кровоизлияния на коже и видимых слизистых оболочках, возникающие самопроизвольно.
Если уровень тромбоцитов в крови падает ниже 20 000/мкл, то возможно развитие тяжелых желудочно-кишечных кровотечений и кровоизлияний во внутренние органы.
Первичная тромбоцитопения. Идиопатическая аутоиммунная тромбоцитопеническая пурпура
Идиопатическая аутоиммунная тромбоцитопеническая пурпура (ИТП) – аутоиммунное заболевание, характеризующееся разрушением кровяных пластинок под действием аутоантител. При этом продукция кровяных пластинок в костном мозге — нормальная или повышенная. Причина возникновения патологии неизвестна.
Различают острую и хроническую формы течения заболевания. Острая форма характерна для детей, хроническая – для взрослых. Продолжительность заболевания при острой форме не превышает 6 месяцев.
Первичная тромбоцитопения у детей. Острая идиопатическая аутоиммунная тромбоцитопеническая пурпура
Острая идиопатическая тромбоцитопеническая пурпура (острая ИТП) развивается чаще всего у детей в возрасте 2-6 лет через 2-4 недели после перенесенной вирусной инфекции (реже вакцинации). В этом возрасте заболевание встречается с одинаковой частотой у мальчиков и девочек. Однако в период полового созревания девочки заболевают в 2 раза чаще.
Начинается процесс, как правило, бурно. Геморрагический синдром развивается быстро, часто внезапно. Характерными чертами пурпуры у детей являются:
- полихромность (буквально «разноцветность») – на коже можно обнаружить геморрагии различной окраски, от багровых до зеленоватых;
- полиморфность – встречаются как точечные (петехии), так и более крупные элементы (экхимозы);
- несимметричность;
- спонтанность возникновения (новые элементы обнаруживаются утром после сна).
Типичным симптомом острой ИТП являются кровотечения (носовые, из лунки удаленного зуба, у девочек пубертатного периода – маточные). В тяжелых случаях может наблюдаться мелена (дегтеобразный кал, характерный для желудочно-кишечных кровотечений), иногда видимая невооруженным глазом гематурия (содержание крови в моче). В дальнейшем может развиться постгеморрагическая анемия.
Кровоизлияния во внутренние органы и головной мозг встречаются относительно нечасто (2-4% случаев). Предвестниками тяжелых осложнений могут служить высыпания на слизистой оболочке рта, обильная кровоточивость, кровоизлияния в сетчатку глаза.
Приблизительно у 10% детей наблюдается умеренная спленомегалия (увеличение селезенки). Температура тела при отсутствии сопутствующих заболеваний – нормальная.
Длительность течения острой ИТП — 4-6 недель, реже — до 6 месяцев. Прогноз при острой форме заболевания — в целом благоприятен. Спонтанные ремиссии наблюдаются в 80% случаев.
Однако у определенной части больных острая ИТП переходит в хроническую форму. Предрасполагающими факторами к такому течению болезни являются:
- склонность к кровотечениям, наблюдавшаяся за полгода и более до появления криза;
- «беспричинное появление» криза;
- наличие у пациента очагов хронической инфекции;
- лимфоцитарная реакция в костном мозге;
- выраженные и упорные кровотечения в сочетании с генерализованной пурпурой, резистентные к проводимому лечению;
- развитие острой аутоиммунной идиопатической тромбоцитопенической пурпуры у девочек в период полового созревания.
У детей и подростков спонтанные ремиссии возможны и при хронической форме заболевания. В остальном хроническая идиопатическая тромбоцитопеническая пурпура протекает у детей, также как и у взрослых.
Первичная тромбоцитопения у взрослых. Хроническая идиопатическая аутоиммунная тромбоцитопеническая пурпура
 Хроническая идиопатическая тромбоцитопеническая пурпура (хроническая ИТП) развивается, как правило, в возрасте 20 – 40 лет. Женщины болеют значительно чаще мужчин (соотношение мужчин и женщин среди заболевших: 1,2 к 3).
Хроническая идиопатическая тромбоцитопеническая пурпура (хроническая ИТП) развивается, как правило, в возрасте 20 – 40 лет. Женщины болеют значительно чаще мужчин (соотношение мужчин и женщин среди заболевших: 1,2 к 3).
Заболевание развивается постепенно. При этом провоцирующий фактор, как правило, выявить не удается. Некоторые авторы отмечают связь с наличием очагов хронической инфекции (хронический тонзиллит), продолжительный контакт с некоторыми химическими веществами (краски, нитроэмали, пестициды).
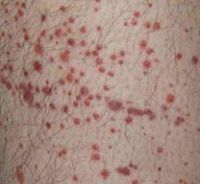
Длительный период заболевание протекает в субклинической форме, и может быть выявлено случайно. Постепенно развивается геморрагический синдром, который может быть различной степени выраженности: от единичных синяков и петехиальных (точечных) внутрикожных кровоизлияний до выраженных кровотечений (кровохарканье, кровавая рвота, кровавый понос, видимая кровь в моче).
Геморрагии на коже располагаются, как правило, на передней поверхности туловища и конечностей. Нередко они появляются на месте инъекций. Кровоизлияния на коже лица, на конъюнктиве и слизистой оболочке губ, свидетельствуют о тяжелом течении заболевания.
В крайне тяжелых случаях происходят кровоизлияния в сетчатку глаза и головной мозг, развивается тяжелая анемия. Предвестником кровоизлияний в мозг могут быть геморрагические везикулы и буллы (наполненные кровью пузырьки и пузыри) на слизистой оболочке ротовой полости.
Спонтанное самоизлечение у взрослых больных наступает крайне редко.
Тромбоцитопения при беременности
Тромбоцитопения при беременности встречается у 7% женщин и развивается, как правило, в последнем триместре. При этом чаще всего наблюдается снижение количества тромбоцитов до 100 000 – 150 000/мкл, так что клинических проявлений не наблюдается. Лишь у 1% беременных регистрируется тромбоцитопения ниже 100 000/мкл.
Механизм развития данной патологии до конца не изучен. Предполагается, что в таких случаях могут иметь место как неиммунные (тромбоцитопеническое действие эстрогенов), так и иммунные механизмы (образование аутоантител к кровяным пластинкам).
Иммунная тромбоцитопения при беременности может представлять опасность для здоровья ребенка, поскольку антитела могут проникать через плаценту и вызывать разрушение тромбоцитов у плода.
Однако в большинстве случаев тромбоцитопении у беременных прогноз благоприятен – и для матери, и для ребенка. Исключением является тромбоцитопения при эклампсии.
Эклампсия протекает с тромбоцитопенией у 10-35% женщин, а в тяжелых случаях позднего гестоза снижение уровня тромбоцитов наблюдается у каждой. Нередко возникают серьезные осложнения, требующие экстренного вмешательства.
